







 Информация
Статьи
Физиологические аспекты контактной термолазерной терапии с примером элиминации вируса папилломы человека с поверхности шейки матки
Информация
Статьи
Физиологические аспекты контактной термолазерной терапии с примером элиминации вируса папилломы человека с поверхности шейки матки
СТАТЬЯ ИЗ ЖУРНАЛА «ЛАЗЕРНАЯ МЕДИЦИНА» -2013.-Т.17, вып.2
УДК 618.14-085.849.19.015.2:615.832
Ежов В.В.1, Данилейко Ю.К.2, Вторенко В.И.1, Дымковец В.П.1, Маныкин А.А.3, Салюк В.А.2, Салиев А.А.1
Физиологические аспекты контактной термолазерной терапии с примером элиминации вируса папилломы человека с поверхности шейки матки
Yezhov V.V.1, Danilleiko Yu.K.2, Vtorenko V.I.1, Dimkovetz V.P.1, Manikin A.A.3, Saljuk V.А.2, Saliev А.А.1
Physiological aspect of the contact thermolaser therapy for the elimination of human papilloma virus from the uterine surface
1 Государственное бюджетное учреждение здравоохранения «Городская клиническая больница № 52 Департамента здравоохранения Москвы», г. Москва;
2 ФГБУ «НИИ вирусологии им. Д.И. Ивановского» Минздрава России, г. Москва;
3 Институт общей физики им. А.М. Прохорова РАН, г. Москва
Цель: изучение метода лазерного лечения, способного элиминировать ВПЧ высокого онкогенного риска с поверхности шейки матки в контексте профилактики рака шейки маки. Материалы и методы. Пациентке с ВПЧ 16-го типа проведен сеанс контактной термолазерной терапии. Результаты исследования. Последующий процесс заживления шейки матки подтвержден расширенной кольпоскопией и трансмиссионной электронной микроскопией; элиминация констатирована методом ДНК полимеразной цепной реакции. Заключение. Продемонстрированный пример подтвердил факт элиминации папилломавируса и диктует необходимость дальнейшего изучения метода контактной термолазерной терапии. Ключевые слова: лазер, вирус папилломы человека, трансмиссионная электронная микроскопия.
Введение
Всемирная организация здравоохранения определила задачу профилактики рака шейки матки как наиболее приоритетную. Проблема заболевания, ассоциированного с вирусом папилломы человека, приобрела особую значимость в связи с высокой контагиозностью, распространенностью вируса и его онкогенным потенциалом. Проблема диагностики и лечения вируса папилломы человека (ВПЧ) привлекает внимание врачей различных специальностей. Это объясняется высокой частотой данного заболевания, а также способностью некоторых разновидностей ВПЧ инициировать злокачественные процессы [18,20].
Внедрение ВПЧ - инфекции происходит на уровне незрелых клеток слизистой оболочки шейки матки на стыке многослойного плоского и цилиндрического эпителия. Результатом этого внедрения является пролиферация клеток, но без продукции вирусных частиц, поскольку пролиферирующие клетки эпителия не способны поддерживать жизненный цикл вирусов. Полная репликация ВПЧ происходит только в высокоспециализированных клетках многослойного плоского эпителия: поверхностных эпителиоцитах слизистой шейки матки, в участках зон трансформации, метаплазии и резервных клетках. В настоящее время описано порядка 100 типов папилломавирусов. Следует отметить их ткане- и видоспецифичностъ. Различные типы ВПЧ связаны с различными видами поражений. Установлено, что с урогенитальной областью ассоциированы определенные типы ВПЧ. Выделяются вирусы низкого и высокого онкогенного риска [5, 10,24].
Возникает необходимость поиска новых методик специализированного лечения больных с дораковой патологией шейки матки, ассоциированной с папилломавирусной инфекцией, а также пациенток с наличием вирусов папилломы человека высокого онкогенного риска на поверхности шейки матки, без видимой цервикальной патологии. В настоящее время ВПЧ выявляется методами гибридизации и ДНК полимеразной цепной реакции (ПЦР).Все типы ВПЧ подразделяют условно на «кожные» и «слизистые». Приоритетный интерес вызывает группа слизистых ВПЧ, обладающих тропностью к аногенитальному и цервикальному эпителию. По возможности вызывать предраковые и раковые изменения типы папилломавирусов разделяют на типы высокого и низкого онкологического риска. К типам высокого риска относят 16,18,31, 33,39,45, 52, 56, 58-й типы. К типам низкого онкологического риска относят 6, 11, 40, 42,
43, 44-й типы. Вирусы низкого риска вызывают остроконечные и плоские кондиломы и папилломы на коже. Типы ВПЧ высокого онкологического риска выявляются в препаратах с интраэпителиальной неоплазией, преинвазивным и инвазивным раком. Вместе с тем, наличие типов ВПЧ высокого онкологического риска является условным патогенным фактором, многократно повышающим возможность малигнизации. Исследования многих ученых показали зависимость между наличием у больных типов ВПЧ высокого онкогенного риска и частотой возникновения рака шейки матки [18, 20].
Из них ВПЧ 16-го типа является причиной более 50% цервикальных раков, ВПЧ 18-го типа -15-25% и т. д. Онкогенность остальных типов вирусов существенно ниже. Одной из главных причин в развитии цервикальной плоскоклеточной неоплазии шейки матки современная наука отводит ассоциации генитальной инфекции с вирусной инфекцией, совершающих скрытую «агрессию» к эпителию [4, 5, 20].
Современное лечение аногенитальных ВПЧ - поражений направлено либо на разрушение папилломатозных очагов тем или иным методом, либо на стимуляцию неспепифического противовирусного иммунного ответа, возможно также сочетание этих двух подходов. Каждый из существующих методов профилактики и лечения патологии шейки матки имеет свои преимущества и недостатки. Поэтому поиск и разработка принципиально новых методов, а также аппаратуры для реализации этих методов элиминации ВПЧ являются весьма актуальными для проведения более эффективной профилактики рака шейки матки [18-20,
Целью данного исследования явилось изучение метода, способного элиминировать ВПЧ высокого онкогенного риска с поверхности шейки матки в контексте профилактики рака шейки маки.
Материалы и методы исследования
Физиологическая концепция контактной термолазерной терапии (КТЛТ)
КТЛТ - это метод термолазерной проработки ВПЧ инфицированной поверхности шейки матки на определенную глубину, позволяющий полностью или частично элиминировать папилломавирусы высокого онкогенного риска. В опубликованных ранее работах современные исследователи описывают этот эффект [6, 8, 9].
Контроль вирусологической эффективности метода проводится в НИИ вирусологии им. Д.И. Ивановского Минздрава России.
Для решения проблемы элиминации вируса папилломы человека с поверхности шейки матки организациями ООО «Новые энергетические технологии». Институтом общей физики им. А.М. Прохорова РАН и специалистами Городской клинической больницы № 52 г. Москвы предложен и изучается принципиально новый подход использования излучения лазеров для элиминации ВПЧ с шейки матки, обусловленной наличием на ней вирусов папилломы человека высокого онкогенного риска. Для реализации этого метода используют высокоэнергетическое лазерное излучение совместно с гетерогенным препаратом на основе углеродных микрочастиц в жидкой (гелиевой) матрице, наносимым на поверхность патологических участков биоткани непосредственно перед облучением. Параметры лазерного излучения — (мощность до 10 Вт, длина волны излучения 0,98 мкм) выбраны из условия минимального деструктивного воздействия на биоткани в отсутствие гетерогенного препарата. Требование к гетерогенному препарату — максимальное поглощение лазерного излучения. Гетерогенный препарат представляет собой суспензию микрочастиц углерода в матрице (водной или гелиевой среде). Микрочастицы углерода (поглощающие центры) имеют диаметр в диапазоне 3-10 мкм и являются центрами интенсивного поглощения лазерного излучения с последующим преобразованием энергии лазерного излучения в тепловую. Процедура лечения заключается в нанесении гетерогенного препарата с поглощающими микрочастицами углерода на патологически измененные участки биоткани с последующим облучением их лазерным излучением. В модели предложенного лечения аногенитальных поражений, ассоциированных с папилломавирусной инфекцией высокого онкогенного риска, процесс стимулированного лазерным излучением термического некроза биоткани можно разбить на ряд этапов. На первом этапе происходит преобразование энергии лазерного излучения, поглощаемого микрочастицами углерода гетерогенного препарата, в тепловую энергию.
На втором этапе происходит быстрая передача тепла от поглощающих лазерное излучение микрочастиц углерода к матрице, в которой расположены поглощающие лазерное излучение микрочастицы углерода. Нагрев матрицы идет до температуры кипения воды. Далее процесс идет практически при постоянной температуре кипения воды. Фаза испарения водной компоненты суспензии (матрицы) является наиболее длительной и зависит от плотности мощности лазерного излучения. Термическое деструктивное воздействие на клеточную структуру слизистой оболочки шейки матки осуществляется в период этой фазы за счет передачи тепла от матицы, расположенной на ее поверхности.
Глубина, на которую перемещается тепловой фронт вглубь биоткани, зависит от времени контакта испаряющейся водной составляющей связующего материала (матрицы) с биотканью.
С момента испарения водной составляющей суспензии (матрицы) передача тепла от поглощающих лазерное излучение микрочастиц углерода, не имеющих контакта с матрицей, к биоткани практически полностью прекращается. Продолжая поглощать лазерное излучение, эти микрочастицы углерода быстро разогреваются до температуры выжигания и удаляются с поверхности. При удалении поглощающих лазерное излучение микрочастиц углерода поверхность биоткани очищается от нанесенного на нее гетерогенного препарата и поглощение лазерного излучения на данном очищенном участке прекращается, т.к. непосредственно биоткань слабо поглощает лазерное излучение. Этим определяется дозированность теплового воздействия по глубине биоткани. Далее пятно лазерного излучения перемещают на соседний участок биоткани с нанесенным гетерогенным препаратом, и процесс повторяется до его полного удаления (выжигания). После лазерного удаления гетерогенного препарата образуется практически очищенная от красящего вещества поверхность обработанной биоткани. Остатки гетерогенного препарата и участки слизистой оболочки шейки матки, подвергшиеся термическому воздействию в процессе лазерного облучения (как правило, это тонкая коагуляционная пленка), удаляются марлевым тампоном.
Схема лечения представлена на рис. 1.

Во всех случаях лечения не наблюдалось Рубцовых изменений на шейке матки и имело место сохранение ее анатомо-функциональной полноценности, что в значительной степени определяет в последующем состояние репродуктивной системы.
Клинический пример
Пример эффективности элиминации ВПЧ высокого онкогенного риска с поверхности шейки матки приведен ниже.
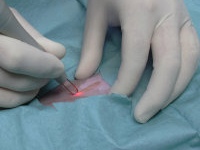
Больная М. 29 лет (см. рис. 2) не работает, в анамнезе 1 беременность в 2008 г. — самопроизвольный аборт(в сроке 5—6 недель) с контрольным выскабливанием матки. Контрацепцию пациентка не применяет. Гинекологический и соматический анамнез не отягощен. На профилактическом гинекологическом осмотре выявлены признаки бактериального вагиноза с ВПЧ 16-го типа. После устранения признаков дисбиоза, в последующем менструальном цикле, при повторном проведении ДНК полимеразной цепной реакции подтвердилось присутствие ВПЧ 16-го типа. На снимке а представлена шейка матки больной до лечения. На б часах имеется небольшой локус дискератоза.
На 7-й день менструального цикла проведен сеанс КТЛТ (см. снимки б—г). Отработанный струп и материал под струпом подвергся ДНК-ПЦР-исследованию и трансмиссионной электронной микроскопии. Слайды д-е - кольпоскопическая картина через 5 недель после КТЛТ. Многослойный плоский эпителий почти полностью восстановился в прежних границах.
После проведения лечения ультраструктура клеток эпителия из цитограммы практически совпадает с нормой (рис. 3), наблюдаются типичные десмосомы. ПЦР, проведенная на этом материале, то есть из биоптатов и мазков пролеченной пациентки, показала отсутствие ДНК папилломавируса. Интерес представлял анализ облученного эпителия, то есть та часть эпителия, которая после воздействия излучения удалялась с поверхности (струп), рис. 3.
При анализе измененной ультраструктуры сопутствующих бактерий, которые присутствуют в материале мазка, было выявлено, что в материале, взятом у больной до проведения лечения, действительно, четко выявляется как внутренняя структура, так и оболочка бактерии, а также структура сопутствующей флоры эпителия шейки матки. Важно отметить, что ДНК бактерии в струпе имеет очень плотный характер, что типично для денатурированной ДНК, в то время как в аналогичных структурах ДНК представляет собой хорошо разрешимые структуры. В облученном материале, методом полимеразной цепной реакции ДНК папилломавирусов не обнаружена. Аналогичная тенденция прослеживается как сразу после лечения, так и через 5 недель после лечения. Через 5 недель (рис. 4) после лечения восстановился эпителий шейки матки. В цитологическом исследовании мазков с поверхности шейки матки признаков атипии и вирусного поражения клеток многослойного плоского эпителия не обнаружено. Исследования продолжаются.

Результаты исследования
У больной на поверхности шейки матки без патологии последней, требующей деструктивного лечения, методом ДНК полимеразной реакции обнаружен ВПЧ 16-го типа, который относится к типам высокого онкогенного риска. В первую фазу менструального цикла пациентке проведена контактная термолазерная терапия.
Результатом лазерного лечения явилась элиминация папилломавирусной инфекции с поверхности шейки матки. Данные исследования подтверждены данными ДНК полимеразной цепной реакции и трансмиссионной электронной микроскопии, взятыми до лечения, непосредственно после сеанса КТЛТ, а также через 5 недель после него.
Контроль за сохранением анатомо-физиологических параметров эпителия шейки матки осуществляли с использованием расширенной кольпоскопии и цитологического исследования мазков. Исследованиями установлено отсутствие признаков ВПЧ-инфекции в цитограммах, тончайших срезах при проведении трансмиссионной микроскопии. Кольпоскопические исследования не выявили грубой цервикальной патологии, а методом ДНК полимеразной цепной реакции констатирован факт элиминации ВПЧ 16-го типа с поверхности шейки матки.

Заключение
Продемонстрированный пример диктует необходимость дальнейшего изучения метода контактной термолазерной терапии. Перспектива лазерной элиминации ВПЧ высокого онкогенного риска с эпителия шейки матки без выраженной травматизации тканей особо важна для пациенток, планирующих продолжение репродуктивной функции. Также проведенная КТЛТ не противоречит популярной в настоящее время вакцинации людей от папилломавирусной инфекции.
Работа ведется под патронажем ООО «Новые энергетические технологии» и выполняется в рамках Государственного контракта № 14.527.12.0011 от 13 ноября 2011 года.
Литература
Поступила в редакцию 09.11.2012 г.
Для контактов: Ежов Виктор Владимирович
e-mail:[email protected]